Aktuality
Lékové interakce antimigrenik – update 2024

Souhrn
Suchopár J, Suchopár Š, Prokeš M. Lékové interakce antimigrenik – update 2024. Remedia 2024; 34: 150–154.
Antimigrenika jsou dynamicky se vyvíjející skupinou léčiv, u které s nárůstem klinických poznatků o účinnosti adekvátně rostou také poznatky o bezpečnosti a lékových interakcích. Tento článek navazuje na dvě předchozí sdělení publikovaná v tomto odborném periodiku věnovaná problematice lékových interakcí antimigrenik. Jakkoliv by se mohlo zdát, že od odevzdání rukopisu uplynuly pouze tři roky a že se za tak krátkou dobu nic významného v oblasti lékových interakcí neudálo, je spíše opak pravdou. Potvrdilo se s definitivní platností, že nová antimigrenika ze skupiny tzv. gepantů představují v oblasti lékových interakcí problém, neboť klinicky významně interagují s inhibitory a induktory CYP3A4, což vyžaduje ze strany lékaře provedení konkrétních intervencí.
Klíčová slova: lékové interakce – antimigrenika – lasmiditan – rimegepant – ubrogepant – fremanezumab – eptinezumab – erenumab – galkanezumab.
Úvod
Od roku 2021, kdy byly v číslech 3 a 4 časopisu Remedia publikovány 1. a 2. část pojednání o lékových interakcích antimigrenik [1,2], došlo k dalšímu rozvoji poznání o bezpečnosti antimigrenik s důrazem na jejich lékové interakce. Smyslem tohoto článku je popsat aktuální stav znalostí o lékových interakcích antimigrenik. Celkem byly od roku 2021 publikovány výsledky více než 20 klinických studií zaměřených na lékové interakce. Některé z nich ukázaly na dosud neznámé vlastnosti antimigrenik, avšak většina z nich potvrdila očekávání a umožnila přesnou kvantifikaci dopadů a případných intervencí, které vedou ke snížení rizika pro pacienty. Došlo také k upřesnění pokynů uvedených v souhrnech údajů o jednotlivých léčivých přípravcích (SPC) a konečně ke změnám došlo rovněž v registraci léčivých přípravků v zemích Evropské unie (EU), když byly po roce 2021 registrovány rimegepant (2022), lasmiditan (2022), eptinezumab (2022) a atogepant (2023).
Rimegepant
Rimegepant byl registrován v únoru 2020 ve Spojených státech amerických pod názvem Nurtec ODT®, tablety o obsahu 75 mg, a následně v květnu 2022 v zemích EU pod názvem Vydura®, orodisperzní tablety o obsahu 75 mg. Držitel rozhodnutí o registraci v poslední aktualizaci SPC uvádí, že není doporučeno souběžné podávání rimegepantu se silnými inhibitory CYP3A4 a se silnými nebo středně silnými induktory. Dále je v SPC uvedeno, že se v případě souběžného podání se středně silnými inhibitory CYP3A4 (např. flukonazolem) nemá podávat další dávka rimegepantu v průběhu dalších 48 hodin a stejný interval je třeba zvolit při souběžném podání silných inhibitorů P‑glykoproteinu (cyklosporinu, verapamilu, chinidinu). Tato doporučení k managementu lékových interakcí jsou v plné shodě s preskripční informací amerického Úřadu pro kontrolu potravin a léčiv (FDA). Ta ale namísto formulace „není doporučeno souběžné podávání“ výslovně uvádí „vyhnout se souběžnému podávání“.
S rimegepantem bylo od roku 2021 publikováno několik studií cílených na lékové interakce. Především bylo prokázáno, že rimegepant v jednorázové dávce 75 mg je prakticky bez vlivu na expozici kombinované hormonální kontracepci založené na ethinylestradiolu a norgestimatu [3], avšak po osmi dnech souběžného podávání dochází ke zvýšení plochy pod křivkou ethinylestradiolu o 20 % (16−25 % na 90% hladině spolehlivosti [90% CI]) a jeho maximálních plazmatických koncentrací o 34 % (90% CI 23−46 %), přičemž současně dochází ke zvýšení plochy pod křivkou norelgestrominu (metabolit norgestimatu) o 46 % (90% CI 39−52 %) a jeho maximálních plazmatických koncentrací o 40 % (90% CI 30−51 %). Autoři studie uvádějí, že změny nejsou příliš klinicky významné, na druhou stranu by takové změny mohly vést, alespoň u některých uživatelek, ke vzniku nežádoucích účinků kontraceptiv, a proto je třeba na takovou možnost myslet.
Další studie, která osvětlovala rozsah změn farmakokinetických vlastností rimegepantu, spočívala v jeho souběžném podávání s inhibitory P‑glykoproteinu, jako je cyklosporin nebo chinidin [4], přičemž cyklosporin je současně inhibitorem jak P‑glykoproteinu, tak i BCRP (breast cancer resistance protein). Ukázalo se, že oba inhibitory zvyšovaly plochu pod křivkou rimegepantu o více než 50 %, avšak méně než dvojnásobně. V případě cyklosporinu došlo ke zvýšení plochy pod křivkou rimegepantu o 60 % (90% CI 49−72 %), obdobná změna byla zjištěna i v případě chinidinu, kde zvýšení plochy pod křivkou činilo 55 % (90% CI 40−72 %). Zatímco v případě cyklosporinu došlo k průměrnému zvýšení maximálních plazmatických koncentrací o 41 %, v případě chinidinu to bylo o 67 %.
Konkrétní dopady výše uvedených zjištění a informací uvedených v SPC vedou k následujícím úpravám dávkování, které jsou uvedeny v tabulce 1.

Za zmínku stojí také výsledky studie, v níž bylo prokázáno, že rimegepant má slabý inhibiční efekt vůči transportním systémům organických kationtů OCT2 a MATE1 [5]. Dvanáctidenní podávání metforminu v dávkách 500 mg 2krát denně spolu s rimegepantem podávaným od 9. do 12. dne v dávkách 75 mg 1krát denně totiž vedlo k mírnému zvýšení plochy pod křivkou metforminu o 17 % (90% CI 11−23 %), přičemž snížení clearance metforminu bylo pozorováno již od 11. dne (tj. po podání 3. dávky rimegepantu). Nebyly zjištěny žádné změny glykemie a autoři dospívají k závěru, že souběžné podávání rimegepantu a metforminu je bezpečné. S takovým závěrem lze jen souhlasit s tím, že je zatím potvrzen pouze pro zdravé dobrovolníky.
Atogepant
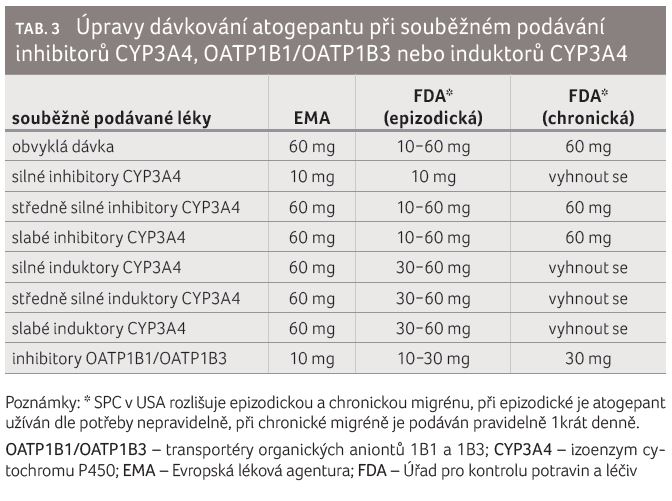
Atogepant byl registrován v USA v září 2021 a v EU v srpnu 2023 pod názvem Aquipta®, tablety o obsahu 10 mg nebo 60 mg. Držitel rozhodnutí o registraci v EU doporučuje v případě souběžného podávání atogepantu se silnými inhibitory CYP3A4 nebo OATP (bez bližší specifikace, mělo by správně být uvedeno OATP1B1/OATP1B3) snížení dávek z obvyklých 60 mg denně na 10 mg denně. Držitel rozhodnutí o registraci v USA odlišuje doporučení úpravy dávky podle toho, zda je atogepant podáván epizodicky jen při migrenózní atace, nebo kontinuálně u chronické migrény. V případě souběžného podávání silných inhibitorů CYP3A4 se u epizodického podávání atogepantu doporučuje dávka 10 mg denně a při chronickém (každodenním) podávání je třeba se podávání atogepantu vyhnout. Na rozdíl od situace v EU platí pro USA odlišná doporučení pro souběžné podávání induktorů CYP3A4. V případě epizodické migrény se mají podávat dávky 30 mg nebo 60 mg a při chronickém podávání je třeba se použití atogepantu vyhnout. Liší se také doporučení pro souběžné podávání inhibitorů OATP1B1, kde v případě epizodického podávání má být užívána dávka 10 mg nebo 30 mg denně, zatímco při chronickém podávání se doporučuje dávka 30 mg denně.
Atogepant je substrátem CYP3A4. Souběžné podávání silných inhibitorů CYP3A4, jako je itrakonazol [11], způsobilo zvýšení plochy pod křivkou atogepantu o 451 % (90% CI 409−496 %) a jeho maximálních plazmatických koncentrací o 115 % (90% CI 95−137 %).
V téže studii u zdravých dobrovolníků [11] byla v části B1 podána jednorázová dávka atogepantu ve výši 60 mg samotná nebo současně s první dávkou rifampicinu ve výši 600 mg. V části B2 bylo pokračováno v podávání rifampicinu v dávkách 600 mg po dobu celkem sedmi dnů, přičemž spolu s šestou dávkou rifampicinu byla podána jednorázová dávka atogepantu ve výši 60 mg. V případě souběžného podání jednorázových dávek došlo ke zvýšení plochy pod křivkou atogepantu o 185 % (90% CI 160−312 %) a jeho maximálních plazmatických koncentrací o 123 % (90% CI 99−150 %). V případě opakovaného podávání rifampicinu došlo ke snížení plochy pod křivkou atogepantu o 61 % (90% CI 56−65 %) a jeho maximálních plazmatických koncentrací o 30 % (90% CI 19−40 %).
Z uvedených výsledků vyplývá, že opakované podávání silného induktoru CYP3A4 snižuje plochu pod křivkou atogepantu o 61 %, což je klinicky významné. Souběžné podávání slabého induktoru CYP3A4 topiramátu [12] vedlo ke snížení plochy pod křivkou atogepantu o 25 % (90% CI 19−31 %) a snížení jeho maximálních plazmatických koncentrací o 24 % (90% CI 15−32 %). V EU na rozdíl od USA není doporučena úprava dávkování při souběžném podávání induktorů CYP3A4. V takovém případě je vhodné se držet doporučení FDA.
Konkrétní úpravy dávkování atogepantu v souvislosti se souběžným podáváním interagující medikace podle SPC v zemích EU a dle FDA SPC v USA jsou uvedeny v tabulce 3.
Podobně jako ubrogepant lze rovněž atogepant bezpečně podávat spolu se sumatriptanem [13], paracetamolem nebo naproxenem [14].
Monoklonální protilátky proti CGRP nebo proti receptoru pro CGRP
Monoklonální protilátky proti CGRP (calcitonin gene‑related peptide) eptinezumab (Vyepti®) registrovaný v USA v únoru 2020 a v EU v únoru 2022, fremanezumab (Ajovy®) registrovaný v USA v září 2018 a v EU v dubnu 2019 a galkanezumab (Emgality®) registrovaný v USA v září 2018 a v EU v únoru 2019 nebo monoklonální protilátka proti receptoru pro CGRP erenumab (Aimovig®) s registrací v USA v květnu 2018 a v EU v srpnu 2018 nemají farmakokinetické lékové interakce a v období let 2021–2024 žádné nové ani nebyly publikovány.
Přehledný článek týkající se lékových interakcí triptanů, ditanů a monoklonálních protilátek [19] potvrzuje, že monoklonální protilátky nemají lékové interakce.
Ostatní antimigrenika a další lékové interakce
Od roku 2021 bylo publikováno několik přehledných prací zaměřených na lékové interakce dalších léčiv používaných při profylaxi nebo terapii migrény, které je vhodné na tomto místě uvést. První z nich byla publikována hned v roce 2021 a je věnována lékovým interakcím léčiv používaných k prevenci migrény [21]. Zaměřuje se na lékové interakce betablokátorů (propranololu, timololu, metoprololu, nadololu a atenololu), protizáchvatových léků (valproátu, topiramátu), antidepresiv (tricyklických antidepresiv, venlafaxinu), kalciových blokátorů (verapamilu, amlodipinu), a dále gepantů (rimegepant a ubrogepant) a monoklonálních protilátek, přičemž podrobně popisuje procesy vstřebávání, metabolizace a role jednotlivých léků jako „victim“ nebo v roli „perpetrator“ lékových interakcí. Také další přehledný článek byl publikován v roce 2021. Věnuje se výhradně lékovým interakcím betablokátorů [22], přičemž mezi „perpetratory“ lékových interakcí uvádí též přírodní látky, jako je kurkumin, ginkgo biloba, zelený čaj, třezalka tečkovaná nebo schizandra čínská, a některé další.
Ze zcela jiného pohledu se na problematiku lékových interakcí zaměřili výzkumní pracovníci společnosti Pfizer z USA [23]. Sledovali celé spektrum léčiv, která užívají pacienti s konkrétními diagnózami (diabetes mellitus 2. typu, obezita a migréna). V případě migrény autoři zjistili, že 64,1 % pacientů užívalo substráty CYP3A, 44,0 % substráty CYP2D6 a 28,9 % substráty CYP2C9. Z uvedených dat následně analyzovali předpokládané skóre dopadu na výskyt potenciálních lékových interakcí a zamýšleli se nad riziky tzv. polyfarmacie, tj. užívání velkého množství léků.
Důsledky lékových interakcí rimegepantu a ubrogepantu na podkladě inhibice nebo indukce CYP3A4 lze snadno modelovat pomocí jednoduchého „kalkulátoru“ dopadu lékové interakce na velikost plochy pod křivkou (https://www.ddi‑predictor.org/predictor/ddi). Zájemci mohou zjistit, že např. souběžné podávání slabého inhibitoru CYP3A4 amlodipinu v dávkách 10 mg denně může zvyšovat plochu pod křivkou rimegepantu o 33 % a ubrogepantu o 55 %. Při porovnání takto vypočtených hodnot s výsledky dosud provedených klinických studií byla zjištěna překvapivě dobrá shoda, a tak lze zájemcům doporučit využít k predikci dopadů lékových interakcí, neboť takový postup vede ke zvýšení bezpečnosti farmakoterapie [24].
PharmDr. Josef Suchopár
DrugAgency, a.s.
Klokotská 833/1a, 142 00 Praha 4
e-mail: suchopar@drugagency.cz
Zdroj: Suchopár J, Suchopár Š, Prokeš M. Lékové interakce antimigrenik – update 2024. Remedia 2024; 34: 150–154.
AJO-CZ-00440

